es la incapacidad para cubrir las necesidades metabólicas de la célula y las consecuencias de esto.
La estrategia general para el tratamiento de estos pacientes ha sido empírica: asegurar una vía respiratoria con ventilación adecuada, y la restauración del volumen vascular además de la perfusión de los tejidos.
Una parte integral del conocimiento del choque es la apreciación de que el cuerpo intenta mantener el estado de homeostasis.
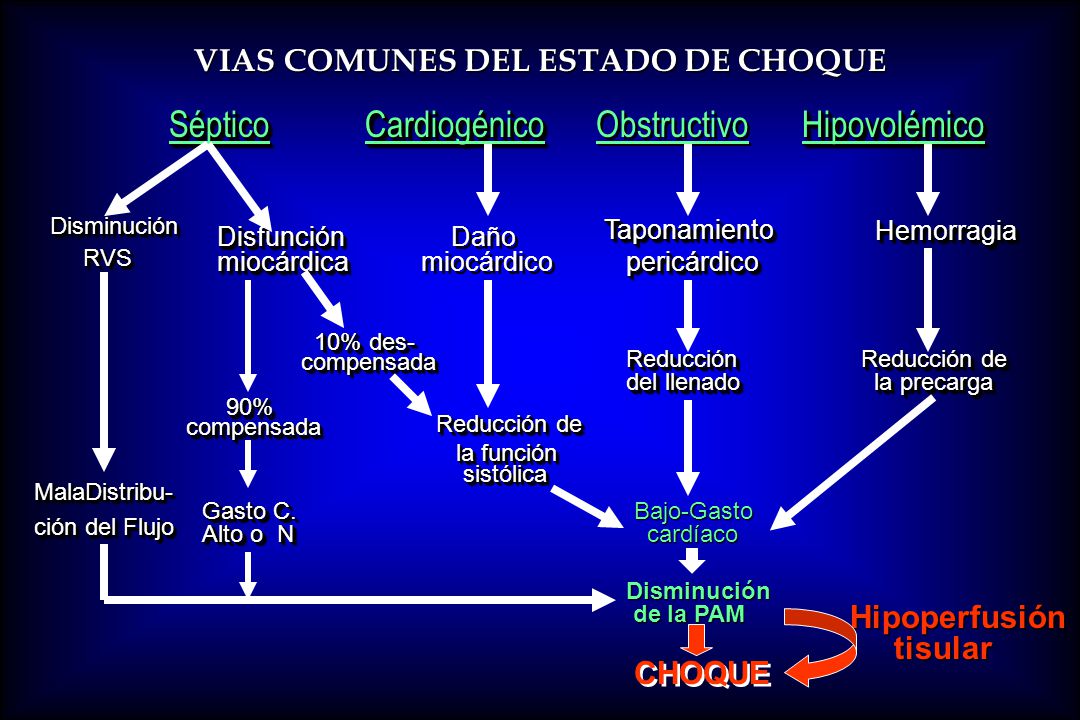
En la práctica clínica reciente se describen seis tipos de choque:
choque hipovolémico: más común, es consecuencia de la pérdida de volumen sanguíneo circulante. Puede deberse a la pérdida de sangre entera (choque hemorrágico), plasma, líquido intersticial (obstrucción intestinal) o una combinación de estos elementos.choque vasógeno atenuación de la resistencia dentro de los vasos de capacitancia, que se observa a menudo en la septicemia.
choque neurógeno es una forma del choque vasógeno en la que la lesión de la médula espinal o la anestesia raquídea causan vasodilatación por pérdida aguda del tono vascular simpático.
choque cardiógeno se atribuye a la falla del corazón como bomba, tal y como sucede en las arritmias o en el infarto agudo del miocardio.
choque obstructivo, causado por embolia pulmonar o neumotórax a tensión, origina una depresión del gasto cardiaco, consecuencia del impedimento mecánico en la circulación, no de una insuficiencia cardiaca primaria.
choque por traumatismo, la lesión del tejido blando y óseo inducen la activación de células inflamatorias y liberación de factores circulantes, como citocinas y moléculas intracelulares que modulan la respuesta inmunitaria.
FISIOPATOLOGÍA DEL CHOQUE
las respuestas fisiológicas iniciales en el choque están impulsadas por la hipoperfusión hística y el desarrollo de déficit de energía celular. Este desequilibrio entre el aporte y las demandas celulares genera respuestas neuroendocrinas e inflamatorias, cuya magnitud casi siempre es proporcional al grado y duración del choque.
Por ejemplo, la respuesta cardiovascular impulsada por el sistema nervioso simpático se amortigua mucho en el choque neurógeno o séptico. Además, puede haber descenso de la perfusión como consecuencia de la activación y disfunción celulares, como en el choque séptico y, en menor medida, en el traumático.
Muchas de las respuestas específicas de los órganos están dirigidas a mantener la perfusión en la circulación cerebral y la coronaria. Éstas se encuentran reguladas en múltiples niveles, incluidos:
a) receptores de estiramiento y barorreceptores en el corazón y vasculatura
b) quimiorreceptores
c) respuestas a la isquemia cerebral
d) liberación de vasoconstrictores endógenos
e) desplazamiento de líquido al espacio intravascular
f) reabsorción y conservación renales de sal y agua.
Respuestas neuroendocrinas y de órganos
específicos a la hemorragia
La finalidad de la respuesta neuroendocrina a la hemorragia es conservar la perfusión al corazón y cerebro, incluso a expensas de otros sistemas y órganos.
Hay vasoconstricción periférica y se inhibe la excreción de líquido.
Existe control autónomo del tono vascular periférico y contractilidad cardiaca, respuesta hormonal a la lesión y el agotamiento de volumen y mecanismos microcirculatorios locales específicos de órganos y reguladores del flujo sanguíneo regional.
El estímulo inicial en el choque hemorrágico es la pérdida del volumen sanguíneo circulante.
Al haber perdida sanguínea se envían señales aferentes al SNC y se activan las respuestas efectoras reflejas o impulsos eferentes, estos tienen como fin expandir el volumen plasmático, conservar el riego periférico y el aporte de oxígeno a los tejidos y restablecer la homeostasis.
Los barorreceptores también son una vía aferente de importancia en el inicio de la respuesta de adaptación al choque. En las aurículas del corazón se encuentran receptores de volumen, sensibles a cambios de la presión de la cámara como al estiramiento de la pared. Se activan con una hemorragia de volumen bajo o disminuciones menores de la presión de la aurícula derecha.
La hemorragia causa reducción del retorno venoso al corazón y disminución del gasto cardiaco. Esto se compensa al incrementar la frecuencia y contractilidad del corazón y asimismo por vasoconstricción venosa y arterial.
Respuesta hormonal
la respuesta a la lesión incluye la activación del sistema nervioso autónomo y la del eje hipotálamo- hipófisis-suprarrenales.
El choque estimula al hipotálamo para producir hormona liberadora de corticotropina, que a su vez activa la secreción de la hormona adrenocorticotrópica por la hipófisis. De manera subsecuente, la ACTH estimula la corteza suprarrenal para liberar cortisol, que actúa de modo sinérgico con la adrenalina y el glucagon para inducir un estado catabólico.
El cortisol :
Estimula la gluconeogenesis
Promueve la resistencia a la insulina en diferentes órganos creando un estado de Hiperinsulinismo
Permite el catabolismo de células musculares y lipolisis para la gluconeogenesis hepatica
Propicia la retención de sodio y agua en las nefronas.
En el choque se activa el sistema renina-angiotensina.
RESPUESTAS INMUNITARIA E INFLAMATORIA
Las respuestas inmunitaria e inflamatoria son un conjunto complejo de interacciones entre factores solubles circulantes y células que surgen como respuesta al traumatismo, infección, isquemia, tóxicos o estímulos autoinmunitarios.
Es un sistema de vigilancia y respuesta continuas que presenta un incremento coordinado después de una lesión para curar al tejido dañado y restaurar el equilibrio hospedador-microbio, además de la supresión activa para regresar a los niveles basales.
Citosinas
NEUTRÓFILOS
También llamados polimorfonucleares son las primeras células que se incorporan en el sitio de lesión.
Eliminan sustancias extrañas, agentes infecciosos, y tejido no viable mediante la fagocitosis.
Cuando estos se encuentran activados también pueden infligir lesión celular y disfunción orgánica.
Se liberan en presencia de isquemia y reanudación del riego y provocan lesión orgánica. Los neutrofilos migran hasta el sitio de lesión donde liberan enzimas proteolíticas como la elastasa, catepsina G y mediadores vasoactivos como leucotrienos y eoicosanoides.
COMPLEMENTO
Los factores del complemento C3a, C4a Y C5a como sabemos son mediadores que incrementan la permeablidad vascular, contraccion del musculo liso,liberacion de histamina y producto accesorio del acido araquidónico.
FORMAS DE CHOQUE
- Choque hipovolémico o hemorrágico
La causa más común de choque en el paciente quirúrgico o traumatizado es la pérdida de volumen circulante por una hemorragia. La pérdida aguda de sangre suscita una disminución refleja de la estimulación barorreceptora de receptores de estiramiento en las arterias grandes, que da lugar a disminución de la inhibición de los centros vasoconstrictores en el tallo encefálico, incremento de la estimulación de quimiorreceptores de los centros vasomotores y disminución del gasto por receptores auriculares de estiramiento. La hipovolemia a su vez induce estimulación simpática, que conduce a la liberación de epinefrina y norepinefrina, activación de la cascada de renina-angiotensina y mayor liberación de vasopresina. Es importante resaltar que la vasoconstricción no está presente en la circulacion coronaria y cerebral para mantener con mayor irrigación esas zonas.
Diagnóstico
Existen signos clínicos en un paciente con choque hipovolemico, como son:
- Extremidades frías y pegajosas
- Taquicardia
- Ausencia o debilidad de pulsos periféricos
- Hipotensión (<110 mmHg)
- Estos signos no suelen aparecer todos de forma simultanea y dependen mucho del volumen de sangre que se ha perdido para que aparezcan. Para esto se tiene una clasificacion hemorragica.
Tratamiento
El componente de la reanimación del paciente en choque es el control de una hemorragia.
Existe prioridades adecuadas en estos enfermos:
a) asegurar las vías respiratorias
b) controlar el origen de la hemorragia
c) reanimación del volumen intravenoso.
Reanimación con control de daño
Dicha estrategia inicia en la sala de urgencias, continúa en el quirófano y en la unidad de cuidados intensivos (ICU).
Las conclusiones razonables en presencia de hemorragia incontrolable incluyen:
- cualquier retraso en la intervención quirúrgica para controlar la hemorragia aumenta la mortalidad;
- en caso de hemorragia no controlada, el intento para alcanzar la presión sanguínea normal podría aumentar la mortalidad, sobretodo con lesiones penetrantes y tiempo de traslado corto;
- una meta de 80 a 90 mmHg para la SBP podría ser adecuada en pacientes con herida penetrante, y debe evitarse la hemodilución profunda
La reanimación con líquidos es un coadyuvante importante para el control físico de la hemorragia en pacientes con choque. En caso de hemorragia grave, la restauración del volumen intravascular debe hacerse con hemoderivados.
La transfusión de concentrados de eritrocitos y otros hemoderivados es esencial para el tratamiento de pacientes en estado de choque hemorrágico. Las recomendaciones actuales en sujetos estables de la ICU incluyen el logro de un nivel de hemoglobina de 7 a 9 g/100 ml.
La reanimación con control de daños y consiste en transfusión con eritrocitos, plasma fresco congelado (FFP, fresh frozen plasma) y unidades de plaquetas administradas en cantidades iguales.
Choque por traumatismo
Reacción sistémica que se da después de un traumatismo que incluye los efectos de lesión de tejidos blandos, fracturas de huesos largos y pérdida de sangre.
Cuando existe traumatismo cerrado es frecuente encontrar insuficiencia de órganos múltiples, incluido el síndrome de insuficiencia respiratoria aguda (ARDS).
La hipoperfusión se incrementa por la activación pro inflamación que ocurre después de la inducción del estado de choque.
Ejemplos de choque por traumatismo:
- Hemorragia pequeña acompañada de lesión de tejidos blandos (fractura de fémur, lesión por aplastamiento)
- Combinacion de choque hipovolémico, neurogéno, cargiógeno y obstructivo que precipite la actividad pronflamatoria.
El tratamiento del choque por traumatismo se dirige a corregir los elementos individuales para atenuar la cascada de activación pro inflamatoria.
Choque séptico (vasodilatador)
Este tipo de choque se caracteriza a diferencia de los otros dos porque hay un estado de vasodilatación periférica con hipotensión resultante y resistencia al tratamiento con vasopresores. Es resultado de la disfunción del endotelio y la vasculatura secundaria a mediadores y células inflamatorios circulantes o como respuesta a la hipoperfusión prolongada grave.
La hipotensión es resultado de la falta de contracción apropiada del musculo liso vascular.
Dentro de las causas de choque vasodilatador, la más frecuente de estas es la septicemia. Pero existen otras causas que difieren de esta última.
- Causas de choque vasodilatador.
La causa más frecuente es la septicemia.
El estado de choque septicémico es un producto secundario de la respuesta corporal a la alteración en el equilibrio entre el microbio y el hospedador, que resulta en una infección localizada invasiva o grave.
Como intento para eliminar los patógenos, las células inmunitarias y de otros tipos (p. ej., endoteliales) elaboran mediadores solubles que acentúan los mecanismos efectores destructores de macrófagos y neutrófilos, aumentan las actividades procoagulantes y de los fibroblastos para localizar a los invasores e incrementan el flujo sanguíneo microvascular para mejorar el aporte de fuerzas destructoras al área de invasión.
En el choque septicémico, los efectos vasodilatadores se deben en parte al aumento de la isoforma inducible de la óxido nítrico sintasa (iNOS o NOS 2) en la pared de los vasos. La iNOS produce grandes cantidades de óxido nítrico por periodos constantes. Este potente vasodilatador suprime el tono vascular y torna resistente la vasculatura a los efectos de fármacos vasoconstrictores.
Diagnostico
Se debe tomar en cuenta las manifestaciones del hospedador e identificación del microorganismo. Se emplean los terminos septicemia, septicemia grave y choque séptico para cuantificar la reacción in-flamatoria del hospedador.
- Criterios de sepsis
SEPTICEMIA
es una respuesta generalizada del organismo (sistémica) grave ante una bacteremia u otra infección.
SEPTICEMIA GRAVE
es una septicemia más una insuficiencia de un sistema esencial del organismo o una irrigación inadecuada a partes del cuerpo debida a una infección.
CHOQUE SÉPTICO
Tratamiento
Tratamiento de primera línea
- Permeabilidad de las vías aereas y ventilación (intubación de ser necesario)
- Reanimacion con liquidos
- Restablecimiento del volumen circulatorio
- Antibioticos empiricos con base a los patogenos mas probables
- Vasopresores
Las catecolaminas son los vasopresores utlizados con mayor frecuencia, pero en personas que tienen resistencia arterial a estas se utiliza la arginia-vasopresina, ya que es una vasoconstrictor potente.
Insulina
Como en personas graves y con septicemia se puede desarrollar hiperglucemia o resistencia la insulina, el uso de esta última como tratamiento ha mejorado el pronóstico del paciente e incluso, reducido las tasas de muerte.
Tratamiento intensivo con insulina (conservación de la glucemia entre 80 y 110 mg/100 ml) o terapia convencional (administración de insulina sólo si las concentraciones de glucosa eran > 215 mg/100 ml, con un objetivo de 180 a 200 mg/100 ml.
Ventilación con menor volumen
Esta implica una corriente inicial de 6ml/kg del peso corporal esperado y presión de meseta de 30 cmH2O o menos.
Corticoides
Se ha demostrado de la utilización de corticoesteoides como una dosis intravenosa única de 50 mh de hidrocortisona, mejoró la respuesta de la presión arterial media a la noradrenalina y fenilefrina en paciente con choque séptico.
Este estudio sugirió que el tratamiento con hidrocortisona no puede recomendarse como coadyuvante habitual para el choque septicémico. Sin embargo, si la SBP permanece < 90 mmHg a pesar de la administración adecuada de líquidos y vasopresores, debe considerarse la hidrocortisona en dosis de 200 mg al día durante siete días divididos en cuatro dosis o en infusión continua.
Choque cardiogénico
El choque cardiógeno se define desde el punto de vista clínico como una falla de la bomba circulatoria que conduce a reducción del flujo anterógrado e hipoxia hística subsecuente, con un volumen intravascular adecuado. Los criterios hemodinámicos incluyen hipotensión sostenida (SBP < 90 mmHg cuando menos durante 30 min), índice cardiaco reducido (< 2.2 L/min/m2) y presión en cuña de la arteria pulmonar alta (> 15 mmHg).
La fisiopatología del estado de choque cardiógeno incluye un ciclo vicioso de isquemia del miocardio que causa disfunción miocárdica y resulta en mayor isquemia del miocardio. Cuando hay necrosis o isquemia de una cantidad suficiente de pared del ventrículo izquierdo y se presenta falla de bomba, disminuye el volumen sistólico. En series de necropsias de fallecidos por choque cardiógeno se encontró daño de 40% del ventrículo izquierdo.99 La isquemia distante de la zona infartada puede contribuir a disfunción sistólica en sujetos con choque cardiógeno. La isquemia del miocardio origina una disminución de la adaptabilidad y se observan, de modo progresivo, incrementos compensadores de las presiones de llenado del ventrículo izquierdo.
La disminución del gasto o la contractilidad cardiaca cuando existe un volumen intravascular adecuado (precarga) puede originar lechos vasculares con disminución de la perfusión y descarga simpática refleja. La mayor estimulación simpática del corazón, por impulsos neurales directos o catecolaminas circulantes, eleva la frecuencia cardiaca, la contracción del miocardio y el consumo miocárdico de oxígeno, que tal vez no se alivien al incrementar el flujo sanguíneo de la arteria coronaria en individuos con estenosis fija de las arterias coronarias. La insuficiencia cardiaca aguda también puede ocasionar acumulación de líquido en el lecho microcirculatorio pulmonar y reducir aún más el aporte de oxígeno al miocardio.
Manifestaciones clínicas
El estado previo al shock de hipoperfusión puede ocurrir con una presión arterial normal.
Cianosis
Presión arterial media y la presión arterial sistólica disminuyen
Gasto urinario disminuido.
Incremento de PVC y PCPC.
Alteraciones de la cognición o del estado de alerta.
Tratamiento
Regulación del volumen liquido
Vigilancia de edema pulmonar y arritmias
Perfusión mediante vasodilatación
tratamiento farmacológico:
VASODILATADORES: decremento de la presión arterial diastólica
Nitroprusiato produce dilatación arterial y venosa, con disminución del retorno venoso al corazón y una reducción de la resistencia arterial.
nitroglicerina dilatación del lecho vascular venoso y en las arterias coronarias
INOTROPICOS POSITIVOS: mejorar la contractilidad cardíaca.
Dobutamina: vasodilatación y una actividad inotrópica positiva.
Milrinona: incremento del transporte de Ca++ hacia las células miocárdicas durante un potencial de acción.
CATECOLAMINAS: aumentan la contractilidad cardíaca, pero, provocan constricción arterial y aumentan la frecuencia cardíaca.
Tratamiento quirúrgico:
Bomba con balón intraaórtica (contrapulsación): refuerza la perfusión coronaria y sistémica, con lo que disminuye la poscarga y la demanda de oxígeno.
Choque neurógeno
El choque neurógeno se refiere a una disminución en la perfusión hística como efecto de la pérdida del tono vasomotor en lechos arteriales periféricos. La pérdida de impulsos vasocons-trictores causa incremento de la capacitancia vascular, disminución del retorno venoso y del gasto cardiaco.
La pérdida de impulsos vasoconstrictores causa incremento de la capacitancia vascular, disminución del retorno venoso y del gasto cardiaco.
La lesión aguda de la médula espinal da lugar a la activación de múltiples mecanismos de una lesión secundaria:
a) alteración vascular de la médula espinal con pérdida de la autorregulación, vasoespasmo y trombosis
b) pérdida de la integridad de la membrana celular y deterioro del metabolismo energético
c) acumulación de neurotransmisores y liberación de radicales
Diagnóstico
La gravedad de la lesión de la médula espinal se correlaciona con la magnitud de la disfunción cardiovascular
La lesión aguda de la médula espinal puede ocasionar bradicardia, hipotensión, arritmias cardiacas, disminución del gasto cardiaco y reducción de la resistencia vascular periférica.
Disminución de la presión arterial acompañada de bradicardia (ausencia de taquicardia refleja por alteración de la descarga simpática)
Extremidades calientes (pérdida de la vasoconstricción periférica)
Déficit motores y sensoriales que indican una lesión de la médula espinal
Tratamiento
Asegurar las vías respiratorias y adecuada ventilación
Reanimación con líquidos y la sustitución del volumen intravascular
Vasoconstrictores mejora el tono vascular periférico, Si la presión arterial del enfermo no responde a una reanimación de volumen adecuada, puede emplearse primero dopamina.
Choque obstructivo
Tratamiento
Quirúrgico: embolectomía pulmonar, pericardiocentesis (taponamiento cardíaco, neumotórax a tensión, hemotórax).
Fármacos fibrinolítico: embolia pulmonar.